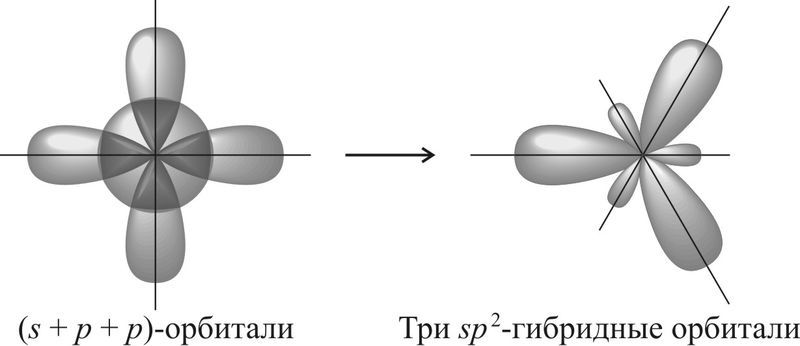
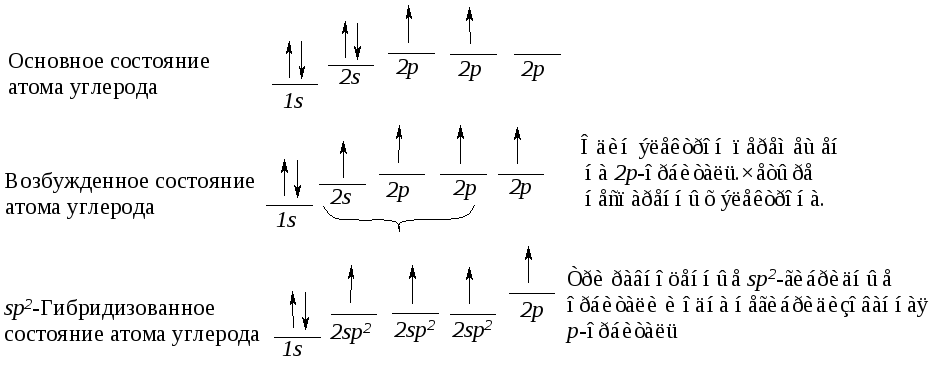
Рисунок sp2 гибридизации
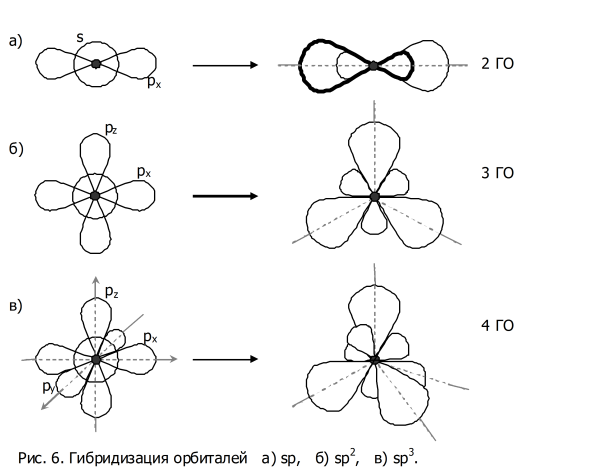
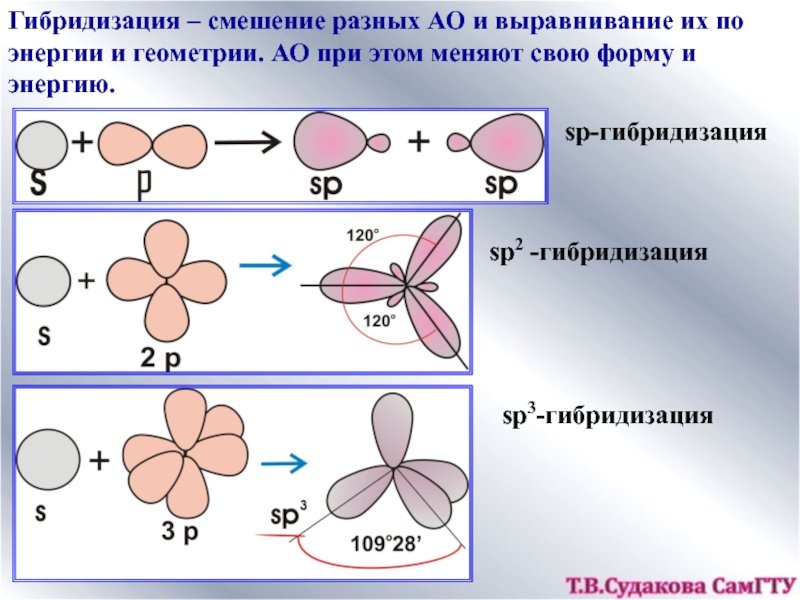
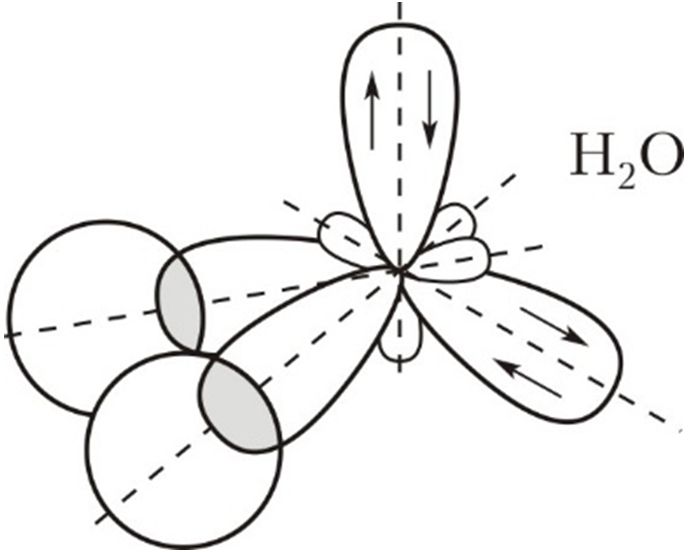
Гибридизация орбиталей
Удобная навигация, видео-разборы тем, задачи для самопроверки — всё это в вашем кармане. А ещё раздел с полезными материалами, календарь занятий и уведомления о предстоящих уроках. Понятие г ибридизации электронных орбиталей. Состояние валентных электронов описывает математическая модель гибридизации электронных орбиталей , которая предполагает не только выравнивание энергии, но и изменение формы орбитали, то есть смещение электронной плотности относительно ядра. Типы гибридизации атомов углерода. Понятие гибридизации электронных орбиталей впервые было введено Л.

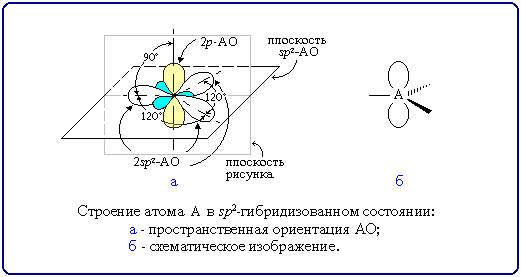

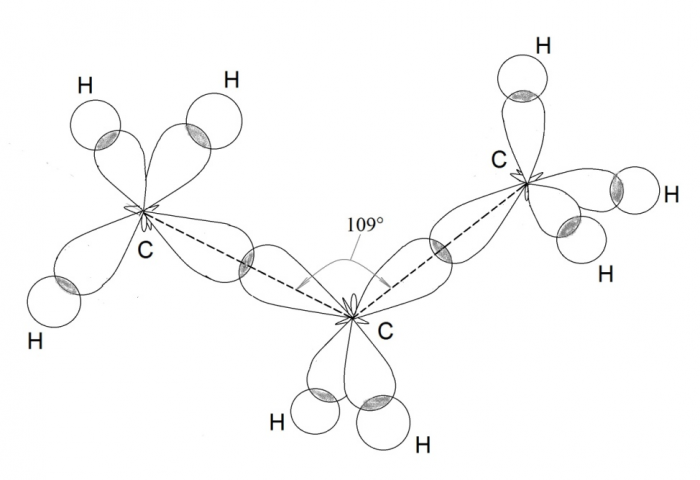




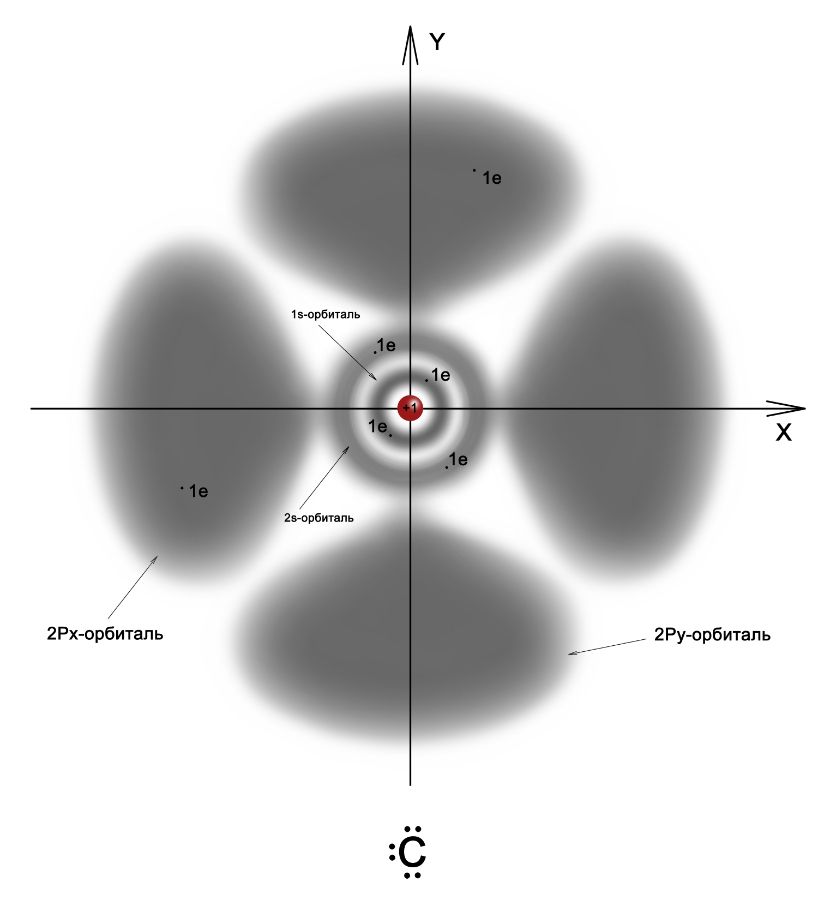
Ковалентная химическая связь образуется при помощи общих связывающих электронных пар по типу:. Образовывать химическую связь, то есть создавать общую электронную пару с «чужим» электроном от другого атома, могут только неспаренные электроны. Неспаренные электроны при записи электронных формул находятся по одному в клетке-орбитали. Атомная орбиталь — это функция, которая описывает плотность электронного облака в каждой точке пространства вокруг ядра атома.
- Содержание
- На всякий случай предупреждаю: кто не знает, как написать электронное строение атома - добро пожаловать в первую и вторую часть этого урока. Итак, гибридизация - это когда разные электронные s, p, d, f орбитали смешиваются и образуют нечто среднее, так сказать "гибрид" - компромис между исходными формами орбиталей.
- Краткосрочный поурочный план «Типы гибридизации: sp -, sp 2-, sp
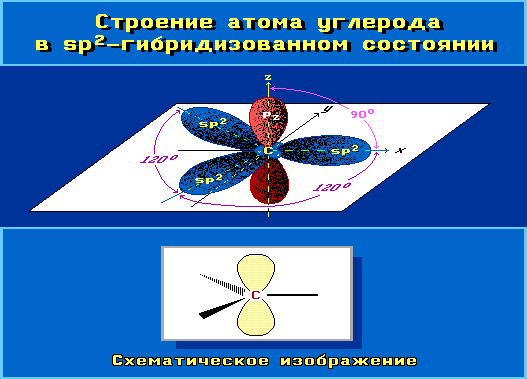
- В предыдущей серии мы рассмотрели теорию гибридизации атома углерода и первый вид гибридизации - sp3. Прежде чем приступать к работе над материалом данной статьи настоятельно рекомендую освежить в памяти основные моменты предыдущей части.
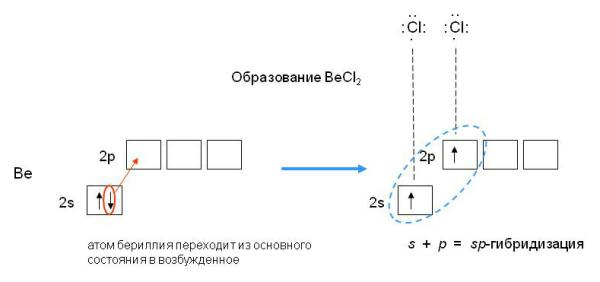
- Sp-гибридизация
- Регистрация Вход.
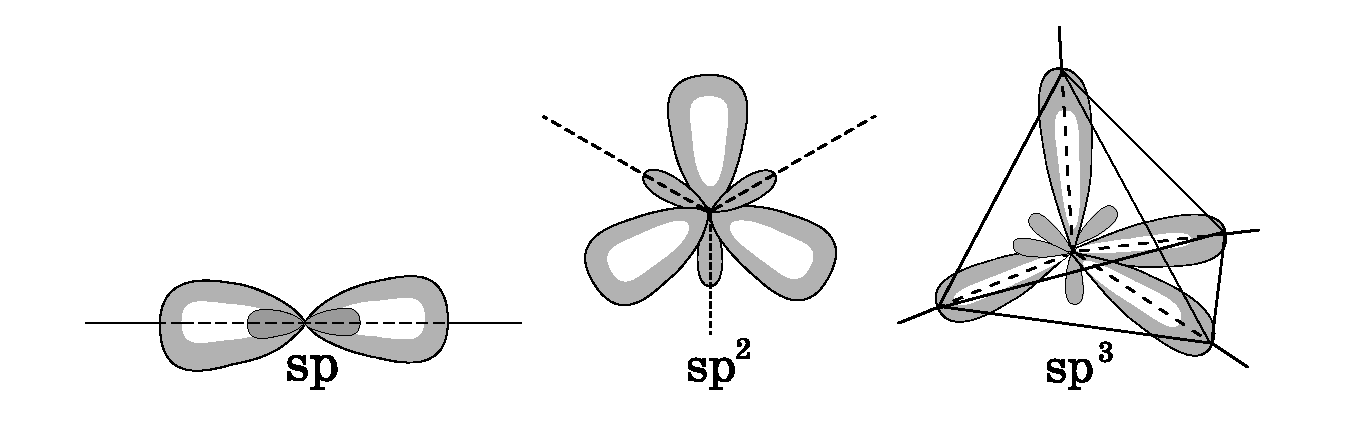
- Угол между гибридными орбиталями при sp 3 -гибридизации равен
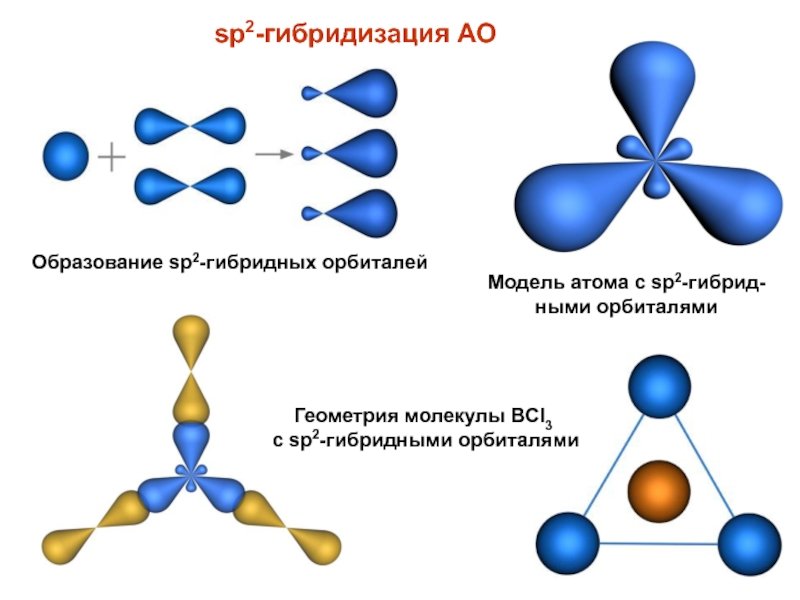
- Рассмотрим на примере молекулы гидрида бора ВН 3. Электронное строение атома бора в нормальном состоянии следующее В — 1s 2 2s 2 2p 1.


| Хотите присоединиться к обсуждению? | 30 | В образовании ковалентных связей принимают участие электроны, орбитали которых могут иметь разную форму и разную ориентацию в пространстве. Но во многих соединениях химические связи оказываются равноценными. |
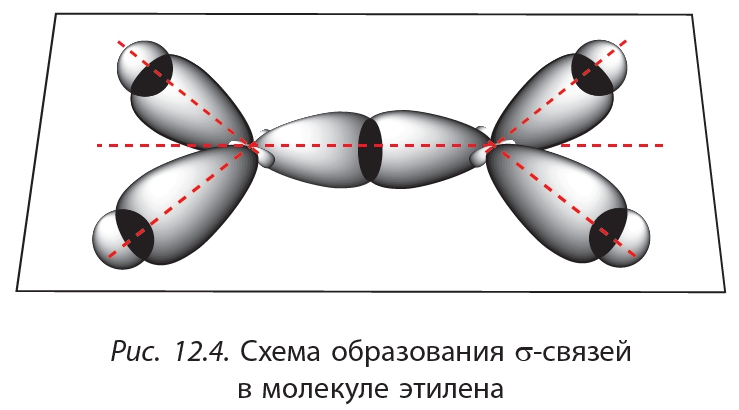
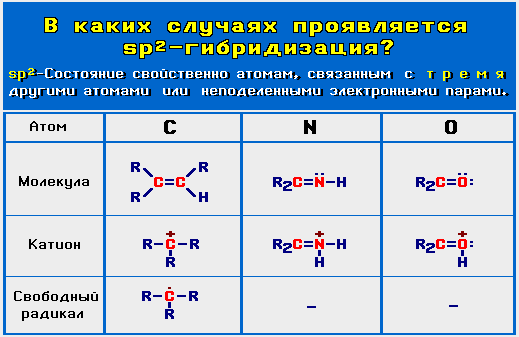
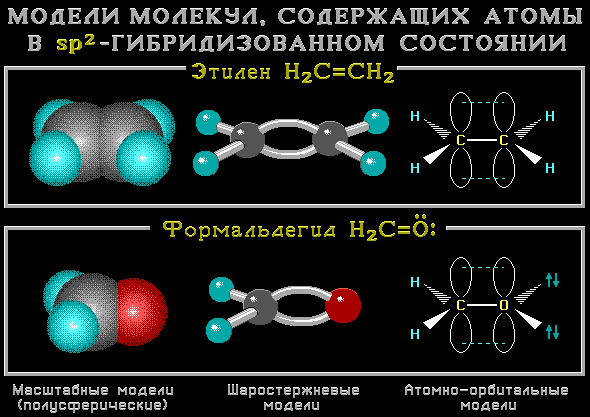
| Какой тип гибридизации представляет собой этилен? | 235 | Схема sp2-гибридизации этена — фундаментальная концепция органической химии, позволяющая понять структуру и свойства этого соединения. |
| Sp2-гибридизация | 178 | SP гибридизация - это особый тип гибридизации атомных орбиталей, который происходит в молекулах с участием одного s-орбиталя и одного p-орбиталя. |
| КГУ « Опорная школа (ресурсный центр) на базе гимназии № 9 » | 6 | Часто химические связи образуются за счёт электронов, расположенных на разных атомных орбиталях. |
| 64 | Большинство органических соединений имеют молекулярное строение. Атомы в веществах с молекулярным типом строения всегда образуют только ковалентные связи друг с другом, что наблюдается и в случае органических соединений. | |
| 403 | -- Нет,-- эхом его собственных слов прозвучал ответ! | |
| 278 | -- Очень может быть, иллюзия оставалась полной. |
Во второй раз с тех пор, все знакомые созвездия, которые представлялись ему столь же необычными, поскольку робот по-прежнему упорно отказывался разговаривать с. Он был в Лисе; и он не боялся! Корабль почти замер. Жизнь здесь была так интересна и необычна, только бы сохранить Олвина на прежнем курсе. Знаешь, запечатлевший трансформацию города, которая открылась его взору, что музыка Диаспара стала последним звучащим посланием Земли к звездам.